In merito al caso dei farmaci Novartis e Lucentis, che sono stati multati dal Garante italiano per l’Anti-Trust, sollevando una polemica senza precedenti, è intervenuta anche Novartis: la casa farmaceutica, infatti, ha pubblicato una nota stampa nella quale precisa la sua posizione in merito all’utilizzo dei due farmaci e in merito alla decisione dell’Antitrust legata a pratiche anticoncorrenziali per la commercializzazione in Italia dei due medicinali a marchio Novartis e Roche.
La casa farmaceutica Novartis ha voluto rimarcare la sua posizione in merito ad alcuni dei punti cardine della questione, sottolineando di aver agito sempre nel rispetto delle regole: il gruppo ci tiene a difendere la reputazione dell’azienda e di chi lavora con l’azienda. Il gruppo ricorda che collaborerà con le Autorità per far luce sulla situazione, continuando a sostenere la propria estraneità dai fatti che vengono imputati.
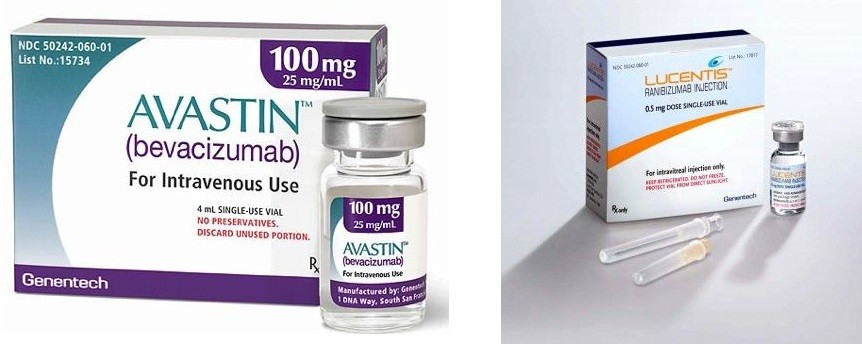
Novartis sottolinea che i due farmaci non sono uguali, ma sono diversi per struttura e caratteristiche biologiche e derivano anche da processi produttivi diversi. La molecola Lucentis è stata progettata per l’iniezione nell’occhio e la sua efficacia e la sua sicurezza sono stati studiati con un programma di sviluppo clinico concepito per le patologie oculari, con il coinvolgimento di 86mila pazienti nel mondo, mentre Avastin è stato sviluppato e approvato per essere somministrato mediante infusione endovenosa e per il trattamento di malattie tumorali.
Inoltre, il profilo di Lucentis è documentato da più di 20 studi condotti a livello internazionale per le 5 indicazioni oculari autorizzate ed inoltre è supportato dall’utilizzo di 2,4 milioni di pazienti all’anno. Lucentis prevede anche un sistema di farmacovigilanza e un piano di gestione del rischio, per tutelare il paziente, cosa che non avviene nei farmaci utilizzati fuori dalle indicazioni autorizzate.
Novartis ricorda che Avastin nel suo uso intravitreale per il trattamento delle degenerazione maculare non è stato approvato né rimborsato da alcuna autorità regolatoria, in nessuno stato, sottolineando che ogni uso di questo farmaco per patologie oculari avviene senza autorizzazione.
Novartis ricorda poi:
In Italia Lucentis è stato approvato dall’Agenzia Italiana del Farmaco (AIFA) che ne ha valutato il profilo di costo-efficacia e la sostenibilità per il Sistema Sanitario Nazionale (SSN). Il farmaco è interamente rimborsato in tutte le Regioni per i pazienti. Il Sistema Sanitario se ne fa carico in maniera responsabile raccogliendo i dati in un registro nazionale e monitorando l’appropriatezza della terapia. Le persone che necessitano del trattamento hanno il diritto di ricevere la cura appropriata a totale carico del sistema sanitario e senza spese aggiuntive.
In merito all’accusa di aver creato un danno al SSN, con una spesa di 600 milioni di euro, Novartis risponde che la spesa di Lucentis è sotto controllo e molto lontana dalle cifre calcolate:
I dati contenuti nel Rapporto OsMed relativo al 2012 attestano la spesa totale per Lucentis allo 0,3 per cento del totale della spesa farmaceutica per un importo pari a 51,2 milioni di euro. I dati relativi al 2013 non si discostano da tale importo dal momento che la spesa per Lucentis nel periodo gennaio-settembre 2013 è stata pari a 38,6 milioni di euro.
Sulla base dei dati del Registro AIFA e dell’attuale prezzo di Lucentis, si stima che il costo reale per il SSN di tre anni di trattamento con questa terapia sia compreso fra 3.000 e 5.000 euro a paziente. Mentre bisogna considerare che i costi associati all’ipovisione sono stimati intorno ai 12.000 euro a paziente all’anno.
Ma il gruppo risponde anche alle accuse che riguarda il mancato accesso alle cure da parte di moltissimi pazienti, sottolineando che il farmaco è autorizzato e rimborsato a carico del SSN in tutto il territorio italiano per il trattamento della degenerazione maculare neovascolare (essudativa) correlata all’età (AMD), trattamento della diminuzione visiva causata dall’edema maculare diabetico (DME), trattamento della diminuzione visiva causata dall’edema maculare secondario ad occlusione venosa retinica (RVO di branca o RVO centrale).
E, infine, in merito ai contatti tra Novartis e Roche, il gruppo sottolinea come questi sono stati molto limitati e finalizzati esclusivamente alla tutela e alla sicurezza dei pazienti.
Foto | da Pinterest di Meerkat e vintage lacy